-
-
2022甘肃高考化学冲刺试卷
可能用到的相对原子质量:H:1 O:16 Si:28 Fe:56 Cu:64 Zn:65 Ag:108
一、单选题:本题共包括16小题,每小题3分,共48分。
1.“新基建”成为2020年的网络热词,包括5G基站建设、特高压、城际高速铁路和城际轨道交通等领域,其中涉及到各类材料。下列说法不正确的是( )
A.高铁列车使用的不锈钢属于合金
B.基础设施建设所用水泥属于硅酸盐
C.5G通信网络所用的光纤光缆材料是SiO2
D.电缆绝缘层所用聚氯乙烯可发生加成反应
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.pH=1的硫酸溶液1L,溶液中含SO![]() 的数目等于0.1NA
的数目等于0.1NA
B.60g SiO2晶体中Si-O键数目为2NA
C.18 g D2O中含有的质子数为10NA
D.真空密闭容器中充入0.1molH2和0.1molI2充分反应后,容器内分子总数为0.2NA
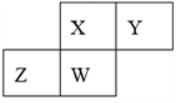 3.短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
3.短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:X>W>Z
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素X、Z、W的最高化合价分别与其主族序数相等
4.下列有关说法正确的是( )
A.纯银器表面在空气中因电化学腐蚀渐渐变暗
B.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
C.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
D.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
5.已知离子电荷相同时,离子半径越小,离子键越强。根据 M/M2O(M=Li、Na)体系的能量循环图,下列判断正确的是( )
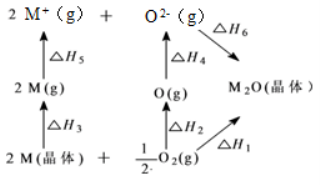 A.ΔH2<0 ΔH4>0
A.ΔH2<0 ΔH4>0
B.ΔH1>ΔH4 + ΔH5 + ΔH6
C.ΔH6(Na2O)<ΔH6(Li2O)
D.ΔH5(Na2O)>ΔH5(Li2O)
6.下列由实验得出的结论正确的是( )
选项 | 实 验 | 实验结论或解释 |
A | 向2mL 0.1mol/L FeCl3溶液中滴加0.1mol/L KI溶液5~6滴,充分反应后,再滴加几滴0.01mol/L KSCN溶液,出现血红色溶液。 | Fe3+与I-之间的反应属于可逆反应 |
B | 探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度 | 则测得的反应速率偏高 |
C | 分别向装有2mL 0.1mol/L H2C2O4溶液和2mL 0.2mol/L H2C2O4溶液的两支试管中加入4mL 0.01mol/L酸性KMnO4溶液,振荡,后者溶液先褪色。 | 探究浓度对反应速率的影响 |
D | 将石灰石与盐酸反应产生的气体直接通入水玻璃中,生成白色沉淀 | 非金属性: C >Si |
7.生产环氧乙烷(![]() )的反应为: 2CH2=CH2(g) + O2(g) 2
)的反应为: 2CH2=CH2(g) + O2(g) 2 ![]() (g) △H=-106 kJ/mol
(g) △H=-106 kJ/mol
其反应机理如下: ① Ag + O2→AgO2慢 ② CH2=CH2 + AgO2→![]() +AgO 快
+AgO 快
③ CH2=CH2 + 6AgO→2CO2+2H2O+6Ag 快 下列有关该反应的说法正确的是( )
A.反应的活化能等于 106 kJ/mol B.AgO2也是该反应的催化剂
C.增大乙烯的浓度能显著提高环氧乙烷的生成速率 D.该反应的原子利用率为100%
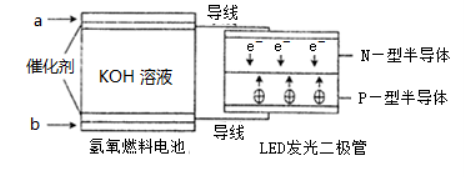 8.LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
8.LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是( )
A.a外通入氧气,b处通氢气
B.通入H2的电极发生反应:H2−2e−===2H+
C.通入O2的电极发生反应:O2+4e−+2H2O===4OH−
D.该装置将化学能最终转化为电能
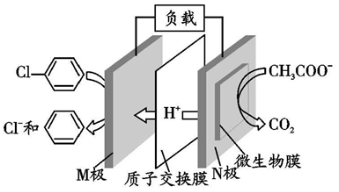 9.含氯苯的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是( )
9.含氯苯的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是( )
A.氯苯被氧化生成苯
B.N极为电池的负极
C.M极电极反应式为:C6H5Cl +e-=Cl-+ C6H6
D.每生成1 mol CO2,由N极区进入M极区的H+为3mol
10.工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有(不考虑氯气的溢出):
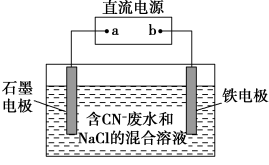 ①CN--2e-+2OH-=CNO-+H2O
①CN--2e-+2OH-=CNO-+H2O
②2Cl--2e-=Cl2↑
③3Cl2+2CNO-+8OH-=N2+6Cl-+2CO+4H2O
下列说法正确的是( )
A.铁电极上发生的反应为Fe-2e-=Fe2+
B.通电过程中溶液pH不断增大
C.除去1 mol CN-,外电路至少需转移5 mol电子
D.为了使电解池连续工作,需要不断补充NaCl
11.甲装置中所含的是物质的量之比为1∶2的CuSO4和NaCl的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是( )
A.是该混合溶液中的SO42-导致了A点溶液的pH值小于B点
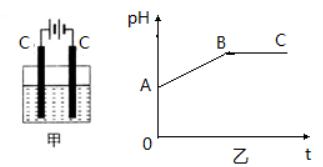 B.整个电解过程中,阴极和阳极产生的气体体积之比大于2
B.整个电解过程中,阴极和阳极产生的气体体积之比大于2
C.AB线段与BC线段在阴极上发生的反应是相同的即:Cu2++2e-===Cu
D.在整个电解的过程中不会出现少量的Cu(OH)2沉淀
12.根据下列图示所得出的结论正确的是()

13.将一定量的氨基甲酸铵置于恒容真空密闭容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g).判断该分解反应已经达到化学平衡的是( )
A.v(NH3)= 2v(CO2)
B.密闭容器中c(NH3):c(CO2)=2:1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
14.工业上,可采用还原法处理尾气中NO,其原理:2NO(g)+2H2(g) N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
实验 | c(NO)/mol·L-1 | c(H2)/mol·L-1 | v(正)/mol·L-1·min-1 |
① | 0.10 | 0.10 | 0.414k |
② | 0.10 | 0.40 | 1.656k |
③ | 0.20 | 0.10 | 1.656k |
下列有关推断正确的是( )
A.上述反应中,正反应活化能大于逆反应活化能
B.若升高温度,则k(正)增大,k(逆)减小
C.在上述反应中,反应级数:m=2,n=1
D.在一定温度下,NO、H2的浓度对正反应速率影响程度相同
15.N2O5是一种新型硝化剂,在一定温度下可发生以下反应2 N2O5 (g)![]() 4NO2 (g) +O2 (g)△H= +Q kJ/mol(Q>0),一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2 (g) +O2 (g)△H= +Q kJ/mol(Q>0),一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c (N2O5) /mol/L | 1.0 | 0.7 | 0.5 | 0.5 |
下列说法中正确的是( )
A.500s时O2的浓度为0.35 mol/L
B.l000s肘将容器的体积缩小一半,重新达到平衡时0.5mol/L< c (N2O5)<1.0 mol/L
C.平衡后,升高温度,正反应速率先增大后减小至平衡
D.相同温度下,若起始充入了参与反应的三种气体各0. 5mol/L,则反应逆向进行
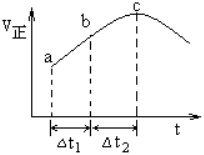 16.向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)
16.向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示,由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示,由图可得出的正确结论是( )
A.反应在c点达到平衡状态
B.△t1=△t2时,SO2的转化率:a~b段小于b~c段
C.反应物浓度:a点小于b点
D.反应物的总能量低于生成物的总能量
17.为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:
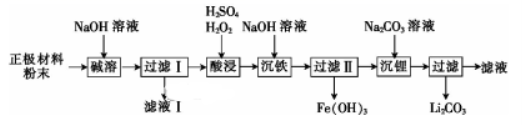
已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为 。
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程: 。
(3)“酸浸”时,溶液中Fe2+发生反应的离子方程式为 。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是 。
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有 。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是 。
18.某化学兴趣小组设计装置,进行实验探究KMnO4与浓盐酸的反应。
[实验1]设计如图1所示装置,并验证氯气的漂白性。
(1)利用装置C验证氯气是否具有漂白性,则装置中I、II、III处依次放入的物质可能是______。
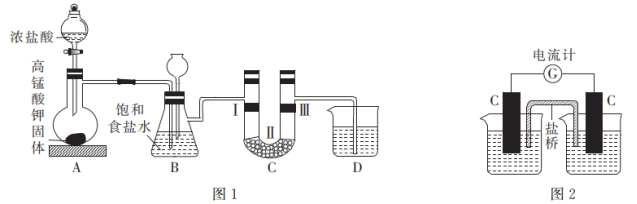
[实验2]设计如图2所示装置,左侧烧杯中加入100 mL由2.00 mol·L-1 KMnO4和6 mol·L-1 H2SO4组成的混合溶液,右侧烧杯中加入100 mL 5.00 mol·L-1 BaCl2溶液,盐桥选择KNO3琼脂。
(2)若用98%的浓硫酸(密度为1.84 g·cm-3)配制500 mL 6 mol·L-1的稀硫酸时,除了需用到玻璃棒、烧杯、量筒之外,还必须用到的玻璃仪器为____________;下列操作会导致所配溶液浓度偏小的是____________(填字母)。
A.容量瓶内壁附有水珠却未干燥处理
B.加水定容时俯视刻度线
C.颠倒摇匀后发现凹液面低于刻度线又加水补足
D.稀释过程中有少量液体溅出烧杯外
(3)左侧烧杯中石墨电极上的电极反应式为________________________________;盐桥中的K+移向____________ (填“左”或“右”)侧烧杯的溶液中。
(4)实验发现,其他条件不变,改用10.0 mol·L-1 H2SO4时,生成氯气的速率比使用6 mol·L-1 H2SO4时快且产生的气体体积更大,其可能的原因是______________________________。
19.现用如图1装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
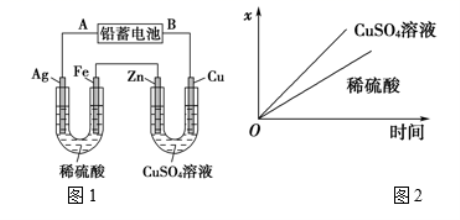
(1)A是铅蓄电池的________极,铅蓄电池正极反应式为: 。
(2)Ag电极的电极反应式是 ,该电极的电极产物共________g。
(3) Cu电极的电极反应式是_______,CuSO4溶液的浓度______(填“减小”“增大”或“不变”)。
(4)如图2表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示_______。
a.各U形管中产生的气体的体积 b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
20.氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N2(g)+2O2(g) 2NO2(g) △H1=+67.0 kJ/mol
2NO2(g) O2(g)+2NO(g) △H2=+116.0 kJ/mol
若某反应的平衡表达式为K=c2(N2)·c2(O2) / c4(NO),请写出此反应的热化学方程式____;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为
(2) 汽车尾气净化反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
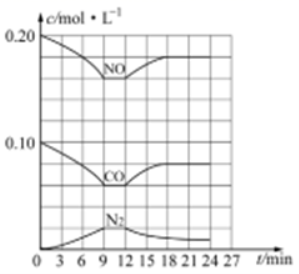
①该反应能自发进行的条件为 (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)= mol·L-l·min-1;
③第12min时改变的反应条件为 ;
④该反应在第24min时达到平衡,此时体系的总压强为P0,此时反应的平衡常数Kp= _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N2 各0.060mol,平衡将 移动(填“正向”、“逆向”或“不”)。
·1·